Il Centro di Fertilità e di Procreazione Medicalmente Assistita della Clinica Polispecialistica San Carlo, accreditato come Centro di III Livello, offre trattamenti di fecondazione assistita (omologa ed eterologa), comprese le inseminazioni intrauterine (IUI), le tecniche di II livello (FIVET e ICSI) e le tecniche di III livello per il recupero chirurgico di spermatozoi testicolari mediante tecnica TESE e microTESE, la preservazione della fertilità.
La nostra equipe, composta da ginecologi, andrologi, ostetriche, biologi, genetisti ed endocrinologi, fornisce un’assistenza di alta qualità, utilizzando tecnologie all’avanguardia per ottimizzare le possibilità di gravidanza.
Siamo specializzati nella gestione dell’infertilità maschile ad alta complessità, affrontiamo condizioni come l’azoospermia non ostruttiva, avvalendoci di test seminologici avanzati e percorsi terapeutici mirati. Offriamo inoltre la crioconservazione dei gameti, utile per preservare la fertilità in pazienti a rischio o per chi desidera posticipare la genitorialità.
Le prestazioni sono disponibili sia in convenzione con il Sistema Sanitario Nazionale che in regime privato. Il nostro Centro è strutturato anche per poter gestire, nel modo più adeguato, i casi di coppie provenienti da altre Regioni. Durante la prima visita, definiamo un progetto di cura personalizzato, assicurando un percorso diagnostico e terapeutico adeguato alle esigenze di ogni coppia.
Cos'è l'Infertilità Femminile
L’infertilità femminile è una condizione clinica caratterizzata dalla difficoltà o impossibilità di ottenere una gravidanza dopo 12 mesi di rapporti sessuali regolari e non protetti. Nelle donne con età superiore ai 35 anni, la valutazione specialistica è generalmente consigliata già dopo 6 mesi di tentativi.
Si tratta di una condizione relativamente frequente che può dipendere da diversi fattori che coinvolgono l’apparato riproduttivo femminile.
Presso il Centro PMA della Clinica Polispecialistica San Carlo ogni coppia viene valutata con un percorso diagnostico personalizzato.
Le cause più frequenti di Infertilità Femminile
- Età e riduzione della riserva ovarica
Soprattutto dopo i 30-35 anni, si verifica una progressiva riduzione della riserva ovarica, cioè del numero e della qualità degli ovociti disponibili. Questo processo fisiologico può rendere più difficile il concepimento spontaneo.
- Infezioni dell’apparato genito-urinario
Alcune infezioni, in particolare quelle sessualmente trasmissibili, possono determinare occlusioni tubariche, aderenze pelviche o modificazioni dell’endometrio, ostacolando l’incontro tra ovocita e spermatozoo.
- Patologie ovariche e alterazioni dell’equilibrio ormonali
Tra le cause più comuni di infertilità di tipo ovulatorio vi è la sindrome dell’ovaio policistico (PCOS), caratterizzata da irregolarità mestruali, assenza di ovulazione, aumento degli androgeni e presenza di numerosi piccoli follicoli ovarici.
Anche altre alterazioni endocrine, come disturbi della tiroide o squilibri ormonali, possono interferire con il normale processo ovulatorio.
- Endometriosi
E’ una patologia ginecologica caratterizzata dalla presenza di tessuto simile all’endometrio al di fuori della cavità uterina, ad esempio su ovaie, tube o peritoneo pelvico. Questa condizione può provocare infiammazione cronica, formazione di aderenze e alterazioni anatomiche degli organi pelvici, interferendo con i normali meccanismi della fertilità.
Un inquadramento specialistico consente di valutare la strategia terapeutica più adeguata, che può includere trattamento medico, chirurgico o percorsi di procreazione medicalmente assistita.
- Malformazioni congenite dell’apparato genitale
Alcune anomalie anatomiche congenite dell’utero o delle tube, possono interferire con il concepimento o con il corretto impianto dell’embrione.
- Infertilità idiopatica
In alcuni casi, nonostante un percorso diagnostico completo, non è possibile individuare una causa specifica. Si parla in questi casi di infertilità idiopatica, una condizione che può comunque essere affrontata con strategie terapeutiche mirate.
Prima consulenza e percorso diagnostico
Il percorso diagnostico-terapeutico della coppia viene personalizzato in base alla storia clinica e agli eventuali fattori di rischio presenti.
Durante la prima visita specialistica nella donna viene eseguita un’anamnesi accurata che consente di costruire un quadro il più possibile preciso.
Sulla base di queste informazioni, lo specialista può indicare gli esami più appropriati per individuare le cause dell’infertilità e definire il percorso terapeutico più adeguato.
Quali esami sono utili nella donna?
- Esami ormonali
Gli esami ematici consentono di valutare lo stato generale di salute e il profilo ormonale della paziente. Tra i principali parametri ormonali analizzati vi sono:
– FSH, LH ed estradiolo
– prolattina
– progesterone
– TSH, fT3 e fT4
– AMH e altri marcatori della riserva ovarica
Questi esami, eseguiti nelle diverse fasi del ciclo mestruale, permettono di valutare:
– la riserva ovarica
– eventuali alterazioni ovulatorie
– possibili squilibri endocrini che possono interferire con il concepimento.
- Esami strumentali
– Ecografia pelvica:
È uno degli esami più importanti nella valutazione della fertilità femminile. Permette di studiare la morfologia dell’utero e delle ovaie e di individuare eventuali fibromi, polipi endometriali, malformazioni uterine o cisti ovariche. Consente inoltre di valutare la numerosità dei follicoli ovarici.
– Isterosonosalpingografia
È un esame ecografico che, tramite l’utilizzo di un mezzo di contrasto cioè soluzione fisiologica, consente di valutare la pervietà delle tube di Falloppio e di individuare eventuali ostruzioni o anomalie della cavità uterina.
– Isteroscopia
È una tecnica endoscopica che consente di visualizzare direttamente la cavità uterina e diagnosticare eventuali patologie dell’endometrio.
Ogni coppia in base alla propria storia può necessitare di esami più particolari (ricerca di specifiche mutazioni genetiche, trombofilia e autoimmunità) e per questo sarà valutato un eventuale profilo personalizzato di esami.
Ogni indagine viene prescritta in modo mirato, evitando esami non necessari.
E’ possibile richiedere una valutazione completa della fertilità.
Cos’è la Procreazione Medicalmente Assistita (PMA)?
La Procreazione Medicalmente Assistita (PMA) comprende un insieme di tecniche mediche utilizzate per aiutare le coppie con difficoltà di concepimento ad ottenere una gravidanza.
Il percorso di PMA viene sempre personalizzato sulla base delle caratteristiche della coppia, dell’età della donna, della riserva ovarica e dei risultati degli esami diagnostici.
Le tecniche di PMA si distinguono in:
– PMA omologa
– PMA eterologa
Entrambe vengono proposte dopo una valutazione specialistica approfondita e dopo aver definito il percorso terapeutico più appropriato
PMA Omologa
La PMA Omologa è una tecnica di procreazione assistita che utilizza i gameti (ovociti e spermatozoi) della coppia stessa.
Questa procedura è indicata quando la coppia presenta difficoltà di concepimento legate, ad esempio, ad alterazioni dell’ovulazione, ridotta riserva ovarica, fattore tubarico o fattore maschile lieve o moderato.
Il percorso può comprendere diverse tecniche, tra cui:
– inseminazione intrauterina (IUI)
– fecondazione in vitro (FIVET)
– iniezione intracitoplasmatica dello spermatozoo (ICSI)
Durante la fecondazione in vitro gli ovociti vengono prelevati dalle ovaie dopo una stimolazione ovarica controllata e successivamente fecondati in laboratorio con gli spermatozoi del partner. Gli embrioni ottenuti vengono poi trasferiti nell’utero della paziente per favorirne l’impianto e l’inizio della gravidanza.
L’indicazione alla tecnica più appropriata viene definita dopo una valutazione clinica completa della coppia.
Percorso diagnostico- terapeutico:
– Consulenza specialistica e inquadramento diagnostico-terapeutico: valutazione clinica e della storia della coppia da parte dei nostri ginecologi e andrologi esperti in fisiopatologia della riproduzione con lo scopo di indentificare le cause dell’infertilità, prescrizione degli esami utili all’inquadramento e alla scelta per percorso terapeutico.
– Pianificazione del trattamento: valutazione dei risultati degli esami prescritti, richiesta di ulteriori valutazioni specialistiche e scelta del percorso terapeutico (PMA omologa di I o II o III livello).
– Stimolazione ovarica controllata: accompagnate da un monitoraggio ecografico e ormonale ogni 2-3 giorni al fine di valutare l’andamento della risposta alla stimolazione ormonale
– Prelievo ecoguidato ovocitario: prelievo degli ovociti della partner femminile effettuato mediante monitoraggio ecografico.
– Fecondazione in vitro in laboratorio: inseminazione mediante tecnica FIVET o ICSI degli ovociti prelevati con gli spermatozoi (freschi o scongelati) e successiva coltura in vitro degli embrioni ottenuti.
– Transfer embrionario e test di gravidanza: trasferimento in utero dell’embrione (fresco o scongelato) tramite sottile catetere sotto guida ecografica e successivo test di gravidanza mediante prelievo di sangue.
In ogni fase, il nostro team di Ostetriche è accanto alla coppia per agevolare il percorso e garantirne la migliore comprensione.
PMA Eterologa
La PMA eterologa è una tecnica di procreazione medicalmente assistita che prevede l’utilizzo di gameti (ovociti o spermatozoi) provenienti da un donatore o da una donatrice esterni alla coppia. Questa opzione viene proposta quando non è possibile utilizzare i gameti della coppia oppure quando precedenti trattamenti di PMA omologa non hanno avuto successo.
Il percorso di PMA eterologa può essere indicato in diverse situazioni cliniche, tra cui:
– esiti negativi di precedenti percorsi di PMA omologa
– ridotta o assente riserva ovarica
– menopausa precoce
– assenza di spermatozoi o grave infertilità maschile
– presenza di patologie genetiche trasmissibili
A seconda del tipo di problematica riproduttiva, la PMA eterologa può prevedere donazione di ovociti (eterologa femminile) oppure donazione di spermatozoi (eterologa maschile).
- Eterologa femminile (donazione di ovociti)
Nel caso della donazione di ovociti, gli ovociti provenienti da una donatrice vengono fecondati in laboratorio con gli spermatozoi del partner della paziente mediante tecniche di fecondazione in vitro. Gli embrioni ottenuti vengono successivamente trasferiti nell’utero della donna che porterà avanti la gravidanza e che ha eseguito una preparazione faramcologica specifica.
- Eterologa maschile (donazione di spermatozoi)
Nel caso della donazione di spermatozoi, vengono utilizzati spermatozoi provenienti da un donatore selezionato. Questa procedura può essere indicata quando è presente assenza di spermatozoi (azoospermia) o grave infertilità maschile, oppure quando vi è il rischio di trasmissione di patologie genetiche maschili.
Gli spermatozoi del donatore possono essere utilizzati nell’ambito di tecniche di I livello come inseminazione intrauterina o di II livello nei trattamenti di fecondazione in vitro, in base alla storia clinica della coppia.
Selezione e sicurezza dei donatori
I gameti utilizzati nei percorsi di PMA eterologa provengono da donatori accuratamente selezionati, sottoposti a rigorosi controlli clinici, genetici e infettivologici. Questo processo di selezione ha l’obiettivo di garantire elevati standard di sicurezza e qualità.
La donazione avviene nel rispetto delle normative vigenti e secondo criteri che tutelano sia i donatori sia le coppie che intraprendono il percorso di procreazione assistita. I donatori vengono sottoposti a valutazioni mediche approfondite e a screening per le principali malattie genetiche e infettive.
Nel corso della consulenza specialistica, la coppia riceve tutte le informazioni relative al percorso terapeutico, alle modalità di selezione dei donatori e alle caratteristiche delle tecniche utilizzate.
Crioconservazione ovicitaria
La preservazione della fertilità comprende un insieme di procedure mediche che permettono di conservare ovociti o tessuto ovarico per mantenere la possibilità di avere una gravidanza in futuro.
Queste tecniche possono essere indicate in diverse situazioni, tra cui:
- trattamenti oncologici che possono compromettere la fertilità
- patologie ginecologiche che possono ridurre la riserva ovarica
- condizioni mediche che richiedono interventi chirurgici sulle ovaie
- scelta personale di posticipare la gravidanza (motivazione sociale)
La procedura più utilizzata consiste nella crioconservazione degli ovociti.
Gli ovociti vengono prelevati dopo una breve stimolazione ovarica e successivamente congelati tramite tecniche di crioconservazione avanzate (vitrificazione), che permettono di mantenerli nel tempo.
Quando la donna desidererà intraprendere una gravidanza, gli ovociti potranno essere scongelati e utilizzati nell’ambito di un percorso di Procreazione Medicalmente Assistita.
La preservazione della fertilità rappresenta oggi un’importante opportunità per tutelare il potenziale riproduttivo femminile, soprattutto in situazioni cliniche che possono comprometterlo nel tempo.
Una consulenza specialistica permette di valutare la riserva ovarica e discutere le possibili opzioni di preservazione della fertilità.
Oligo-Asteno-Teratospermia
Nel caso in cui lo spermiogramma presenti alterazione di almeno un parametro (concentrazione degli spermatozoi; percentuale di motilità progressiva; percentuale di morfologia normale) in due esami successivi, opportunamente distanziati di 3 mesi l’uno dall’altro, si parla di infertilità maschile.
- La più comune alterazione del liquido seminale è la oligo-asteno-teratospermia (OAT), ovvero una riduzione del numero degli spermatozoi, della percentuale di motilità e della percentuale di morfologia normale (Manuale WHO, 2021).
Quali sono le cause di infertilità maschile?
- problematiche endocrinologiche, con alterazione dell’asse ormonale che regola l’attività testicolare
- pregresse flogosi testicolari e della via seminale (epididimiti, prostatiti, uretriti,..)
- subostruzioni delle vie seminali, generalmente conseguenti a traumi o processi flogistici
- elevato indice di frammentazione del DNA spermatico
- varicocele
- pregressa storia clinica di criptorchidismo
- pregressi traumi genitali
- pregresse terapie chirurgiche demolitive e/o trattamenti chemioterapici
- anomalie anatomiche congenite delle vie seminali
L’infertilità maschile può essere idiopatica: in questo caso non sono riconosciute cause specifiche della (eventualmente progressiva) riduzione della funzione riproduttiva (riguarda il 30-40% degli uomini infertili).
La valutazione clinica e gli approfondimenti diagnostici sull’uomo infertile che eseguiamo nel nostro Centro possono comprendere:
- test di II e III livello sul liquido seminale (tra cui quello sulla frammentazione del DNA spermatico)
- ecocolordoppler scrotale e, in casi selezionati, ecografia prostatica trans rettale
- dosaggi ormonali: FSH, LH, testosterone totale, prolattina, Estradiolo
- screening genetici: cariotipo; studio del Gene della fibrosi Cistica; ricerca delle microdelezioni del cromosoma Y
Azoospermia e Criptospermia
Il nostro Centro si distingue in particolare per la gestione della Azoospermia, ovvero la assenza di spermatozoi su due campioni di liquido seminale (dopo centrifugazione ed esame del sedimento) distanziati di tre mesi.
La Criptospermia è invece la presenza nel liquido seminale di rari spermatozoi, visibili solo dopo centrifugazione del campione.
Esistono due forme di azoospermia:
- ostruttiva (25-30% dei casi), OA, cioè causata da una ostruzione delle vie seminali che non permette il transito degli spermatozoi, ma che sono prodotti normalmente dai testicoli
- non-ostruttiva (70-75% dei casi), NOA, dovuta cioè ad una problematica testicolare primaria, che comprende diverse alterazioni specifiche della spermatogenesi nei microtubuli testicolari (ipospermatogenesi severa, arresto maturativo completo o incompleto, sindrome a sole cellule di Sertoli, ecc.).
La diagnosi di azoospermia comporta poi accertamenti di approfondimento:
- ecocolordoppler scrotale e, in casi selezionati, ecografia prostatica trans rettale
- dosaggi ormonali: FSH, LH, testosterone totale, prolattina, Estradiolo
- screening genetici: cariotipo; studio del Gene della fibrosi Cistica; ricerca delle microdelezioni del cromosoma Y
In caso di Azoospermia Ostruttiva (OA), può essere valutata la fattibilità di una ricanalizzazione chirurgica della via seminale (per approfondimenti consulta l’argomento Terapia Chirurgica della Azoospermia), da discutersi con la coppia, dopo aver valutato le percentuali di successo dell’intervento (ricomparsa di spermatozoi nell’eiaculato), ma anche lo stato di fertilità della partner femminile.
Nella maggior parte dei casi, tuttavia, vi è indicazione a ricorrere a un recupero chirurgico di spermatozoi testicolari, con agoaspirato testicolare (Testicular Fine Needle Aspiration – TeFNA) o con estrazione chirurgica standard di spermatozoi testicolari (Conventional Testicular Sperm Extraction – cTESE). Si sottolinea, in ogni caso, come la procedura di agoaspirato sia una tecnica ‘alla cieca’, non scevra da complicanze (es.: sanguinamenti interni al testicolo, fibrosi post cicatriziale,…), che non sempre consente di recuperare un adeguato numero di spermatozoi per crioconservazione degli stessi.
In caso invece di Azoospermia Non Ostruttiva (NOA), le Linee Guida internazionali raccomandano di eseguire un prelievo di spermatozoi testicolari con microTESE (microdissection Testicular Sperm Extraction) la quale, rispetto alla TESE convenzionale, presenta, in mani esperte, maggiori tassi di recupero di spermatozoi (45 – 55% rispetto al 25-35% di una TESE) e una minore perdita di tessuto testicolare (con minore impatto sui livelli di Testosterone).
La Criptospermia può riconoscere a sua volta una origine ostruttiva o non ostruttiva, e comporta come minimo la necessità di ricorrere a fecondazione in vitro (ICSI – IntraCytoplasmic Spem Injection).
Qualora il numero e/o le caratteristiche biologiche degli spermatozoi disponibili non risultassero adeguate neppure per l’utilizzo in vitro, vi sarebbe indicazione a prelievo di spermatozoi testicolari mediante TESE o microTESE, a seconda della natura della criptospermia (appunto ostruttiva o non ostruttiva, rispettivamente).
Varicocele
Il varicocele è la dilatazione delle vene del plesso pampiniforme, responsabili del drenaggio del testicolo, a livello inguino-scrotale.
È una condizione che colpisce principalmente il testicolo sinistro (97% dei casi), anche se raramente può presentarsi a destra o bilateralmente.
Il varicocele insorge tipicamente dopo la pubertà (15-25 anni), molto raramente durante l’infanzia ed eccezionalmente dopo la quarta decade di vita.
Le potenziali conseguenze del varicocele sono un aumento della temperatura intratesticolare, la mancata eliminazione di prodotti del metabolismo testicolare e, non ultima, il reflusso di prodotti catabolici prodotti dal rene e dalla ghiandola surrenalica.
Clinicamente il paziente può essere asintomatico o riferire un senso di peso a livello del testicolo; se il varicocele è ben sviluppato, alla autopalpazione il paziente può avere la sensazione, come in modo colorito riporta un libro americano, di palpare come “un groviglio di lombrichi” al di sopra del testicolo.
Numerosissimi studi clinici associano il varicocele ad una qualità dello sperma inferiore alla norma e, nei bambini, ad un minor sviluppo del testicolo omolaterale.
Non esiste terapia medica per questa patologia.
La diagnosi di varicocele viene posta solitamente durante la visita medica, tuttavia risulta indispensabile, per la sua corretta valutazione, eseguire un’Ecografia con Eco-Color-Doppler dei vasi spermatici.
Nei giovani adulti (dai 17-18 anni in su), la valutazione dopo riscontro di varicocele comprende l’esecuzione di almeno uno o due esami qualitativi del liquido seminale, per determinare il livello della fertilità.
Frammentazione DNA spermatico
Negli ultimi anni, è emerso come il solo esame seminale di base (conta, motilità, morfologia degli spermatozoi), non renda conto di tutti gli aspetti della fertilità maschile.
In particolare, sono stati sviluppati test che studiano l’integrità e la maturazione del DNA spermatico: questo parametro può influenzare in varia misura le probabilità di concepimento spontaneo, i risultati delle IUI (inseminazioni intrauterine) e anche della fecondazione in vitro (FIVET e ICSI – Intracytoplasmic Sperm Injection).
Tra tutti questi scenari, i risultati della ICSI risulterebbero meno suscettibili a un elevato tasso di frammentazione spermatica: i risultati in Letteratura sono comunque controversi su questo punto, in dipendenza presumibilmente del livello di frammentazione presente.
I test che vengono eseguiti nel nostro Centro per lo studio della frammentazione del DNA spermatico sono illustrati nella sezione Diagnostica di Laboratorio.
Terapie Ormonali e Nutraceutiche
Le terapie mediche per l’infertilità maschile rimangono in gran parte empiriche, con poche evidenze scientifiche significative a supporto della maggior parte di esse, eccetto che per indicazioni cliniche specifiche.
Le linee guida AUA/ASRM (American Urological Association e American Society for Reproductive Medicine) del 2024 precisano che la terapia medica è raccomandata ed efficace solo nei casi di ipogonadismo ipogonadotropo (deficit nel sangue delle gonadotropine – FSH ed LH, prodotte dall’ipofisi – con conseguente riduzione della spermatogenesi e della produzione di Testosterone da parte dei testicoli). In questo caso, la somministrazione farmacologica delle gonadotropine stesse ripristina entrambe le funzioni.
Laddove non si rilevino invece cause specifiche e reversibili dell’infertilità maschile (OAT idiopatica), sono state proposte terapie ormonali che vanno decise in base alle situazioni particolari e di cui è opportuno discutere con i pazienti mediante adeguato counselling:
- modulatori selettivi dei recettori degli estrogeni (SERM): clomifene citrato, tamoxifene
- inibitori dell’aromatasi (AI): anastrozolo, letrozolo
- goadotropine: gonadotropina corionica (hCG), FSH
L’efficacia di tali terapie risulta comunque modesta, in casi selezionati, quando non incerta, e vanno considerate soprattutto nei pazienti con valori di Testosterone al di sotto della norma poiché possono migliorare il profilo ormonale ripristinando almeno in parte la spermatogenesi. Mancano in ogni caso dati più solidi relativamente al beneficio su tassi di gravidanza e di nati vivi.
La supplementazione con sostanze nutraceutiche, in particolare antiossidanti, ma anche probiotici, vitamine, etc., è largamente utilizzata nelle forme di oligoastenospermia idiopatica, ma recenti studi randomizzati di grandi dimensioni e review sistematiche mostrano effetti incoerenti sulla qualità del liquido seminale e nessun chiaro miglioramento nei tassi di gravidanza a termine.
Anche in questo caso, le linee guida internazionali raccomandano di informare i pazienti sulla dubbia utilità clinica degli integratori e sulla mancanza di indicazioni per specifici componenti.
Nelle forme di OAT causate da parziali ostruzioni delle vie seminali di maturazione e trasporto degli spermatozoi (epididimi, deferenti, prostata,…) di natura post infiammatoria (esiti di pregresse infezioni e infiammazioni del tratto genito-urinario), sono controversi e in ogni caso parziali gli effetti di terapie antibiotiche prolungate e/o antiinfiammatorie (FANS, cortisonici,…), come anche di integratori, le cui implicazioni vanno come sempre discusse con il paziente.
Terapia Chirurgica della Azoospermia: TESE (Testicular Sperm Extraction)
La TESE (Testicular Sperm Extraction) è una procedura chirurgica ‘a cielo aperto’, che viene eseguita in anestesia locale e sedazione, con piccola incisione sulla cute scrotale, apertura degli strati superficiali e accesso alla tunica albuginea del testicolo. Dopo ulteriore piccola incisione di questa, si esegue escissione di piccolo frammento di tessuto testicolare per la ricerca e la crioconservazione degli spermatozoi.
Questa tecnica è indicata sicuramente nelle Azoospermia ostruttiva (OA) e nei casi di oligospermia severa o criptospermia (quest’ultima definibile come la presenza di rari spermatozoi visibili solo dopo centrifugazione del liquido seminale), laddove quindi il numero e/o la qualità dei gameti risultino problematici per una adeguata probabilità di successo con fecondazione in vitro (compresi i casi in cui la coppia abbia già eseguito almeno un ciclo di fecondazione in vitro senza successo, avendo ottenuto bassi tassi di fertilizzazione degli ovociti e/o embrioni di ridotta qualità).
Risulta possibile prendere in considerazione e discutere con la coppia l’eventuale ricorso a TESE anche nei casi in cui sia presente una elevata percentuale di spermatozoi con DNA frammentato – pur con valori seminali basali nella norma -, non suscettibile di miglioramento con terapia medica e/o non valicabile con metodica biologica di selezione degli spermatozoi, e comunque dopo almeno aver proceduto a uno/due cicli di fecondazione in vitro senza successo con spermatozoi da eiaculato (EAA Guidelines on OligoAsthenoTeratospermia, 2018).
- TESE PER CRIOCONSERVAZIONE
La modalità più frequentemente impiegata consiste appunto nel prelievo di spermatozoi testicolari, con Crioconsevazione degli stessi in una serie di dispositivi chiamati “paillettes”. Gli spermatozoi risulteranno quindi successivamente disponibili per l’utilizzo in fecondazione in vitro.
TESE ‘a fresco’ con Pick Up Ovocitario
In casi selezionati, è possibile proporre un prelievo testicolare ‘a fresco’: in questo caso, si procede a contemporaneo prelievo, nella stessa giornata, di spermatozoi da testicolo e degli ovociti nella partner, per procedere a fecondazione in vitro immediata, evitando, sul primo ciclo, il passaggio di crioconservazione e scongelamento degli spermatozoi (naturalmente, i gameti recuperati oltre a quelli utilizzati vengono crioconservati per i cicli successivi). Questa scelta dipende da una serie di considerazioni cliniche legate al numero e alla qualità degli spermatozoi di cui si ipotizza di poter disporre, oltre alla possibilità di sfruttarne al massimo le caratteristiche biologiche nel processo di fecondazione, poiché lo scongelamento successivo – comunque usualmente utilizzato – comporta la perdita di vitalità di una aliquota degli spermatozoi (dal 30 al 50%) e/o un possibile (ma difficilmente valutabile) danno al DNA nucleare (frammentazione del DNA spermatico).
Terapia Chirurgica della Azoospermia: MicroTESE (Microsurgical Testicular Sperm Extraction)
La MicroTESE (Microsurgical Testicular Sperm Extraction) è una tecnica considerata ormai il gold-standard nei casi di Azoospermia non ostruttiva (NOA). La percentuale di pazienti con recupero positivo di spermatozoi riportato in Letteratura e nelle nostre casistiche risulta del 45-58% (rispetto a un massimo del 30-35% con TESE convenzionale).
E’ possibile proporre una MicroTESE (salvage microTESE) anche pazienti già sottoposti a TESE con recupero negativo di spermatozoi: in questi pazienti, la percentuale di successo risulta mediamente del 40%.
La MicroTESE viene eseguita in anestesia generale, la esposizione del testicolo e una incisione della tunica albuginea che consente l’esame approfondito con microscopio operatore (sino a 36 ingrandimenti) del tessuto testicolare (su un testicolo o su entrambi, in base all’esito del recupero in tempo reale): in tal modo, è possibile eseguire microprelievi selettivi delle aree di tessuto che più probabilmente contengono spermatozoi (ovvero, quelle con microtubuli seminiferi di calibro maggiore). Nonostante l’esame del tessuto testicolare sia esteso ed approfondito, questa metodica caratterizzata da microprelievi mirati non comporta danno del testicolo né asportazione di materiale non utile ai fini della ricerca di spermatozoi, risparmiando in particolare le cellule endocrine responsabili della produzione di Testosterone (rispetto alla TESE che, quando impropriamente impiegata in questi pazienti, necessita comunque di una quantità maggiore di tessuto per poter ottenere una pur sempre inferiore probabilità di successo).
Il Biologo lavora in contemporanea in sala operatoria, riferendo in linea diretta presenza o assenza di spermatozoi, la stima numerica e la morfologia degli stessi, mediante esame di aliquote di tessuto prelevato dal chirurgo Andrologo.
Gli spermatozoi recuperati vengono utilizzati per fecondazione in vitro (ovvero la tecnica ICSI, ‘iniezione intracitoplasmatica di spermatozoi’): le percentuali di successo di questo percorso dipendono analogamente dalla lunga e approfondita esperienza del chirurgo Andrologo, dei Biologi, che cercano gli spermatozoi nel tessuto prelevato, e degli Embriologi, che li utilizzeranno per la fecondazione degli ovociti.
- MICROTESE PER CRIOCONSERVAZIONE
Come nel caso della TESE, anche con MicroTESE si è da sempre usualmente proceduto a crioconservazione degli spermatozoi prelevati per successivo utilizzo in fecondazione in vitro.
MicroTESE ‘a fresco’ con Pick Up Ovocitario
Le Linee Guida internazionali suggeriscono che il prelievo di spermatozoi ‘a fresco’ sia da preferirsi in quei pazienti dove il numero degli spermatozoi recuperati sia molto ridotto e quindi risulterebbe problematica la sopravvivenza degli stessi dopo scongelamento (viene riportata in effetti una maggiore sensibilità degli spermatozoi di pazienti affetti da azoospermia non ostruttiva al danno indotto dalla crioconservazione).
Inoltre, è stato evidenziato analogamente come, in presenza di numeri bassi di spermatozoi, si avrà anche una riduzione delle percentuali di successo della fecondazione in vitro, in particolare della live birth rate (percentuale di bimbi nati). In questi pazienti, dunque, utilizzare spermatozoi ‘a fresco’ ottimizza le chances di fertilizzazione ovocitaria e del successivo sviluppo embrionario con percentuali superiori di gravidanze a termine.
Per queste ragioni, negli ultimi anni, nel nostro Centro abbiamo iniziato a lavorare con MicroTESE ‘a fresco’, programmando l’intervento chirurgico in coordinazione con il pick up ovocitario.
Naturalmente, la aliquota complessiva di spermatozoi recuperati, a parte quelli impiegati in fecondazione in vitro ‘a fresco’, viene comunque crioconservata per gli eventuali cicli successivi.
Il rischio di un recupero negativo di spermatozoi anche con microTESE bilaterale (con necessità di crioconservazione degli ovociti) risulta compensato dal poter utilizzare subito in fecondazione gli eventuali rari spermatozoi recuperati.
Tutti i pazienti affetti da azoospermia non ostruttiva rappresentano una sfida complessa per la nostra équipe: non è possibile infatti evidenziare a priori un fattore predittivo assoluto di successo o insuccesso (salvo rare eccezioni), e quindi la proposta di intervenire ‘a fresco’ rappresenta l’opportunità di sfruttare sino in fondo la potenzialità biologiche degli spermatozoi.
Correzione del Varicocele
La correzione del varicocele ha lo scopo di risolvere la dilatazione venosa presente a livello scrotale impedendo al sangue di refluire verso il testicolo.
TECNICHE CHIRURGICHE
La legatura chirurgica della vena spermatica o delle vene del plesso pampiniforme può essere eseguita con diverse tecniche, che vengono praticate dalla nostra equipe andrologica:
- legatura con incisione chirurgica alla spina iliaca: tecnica di Palomo o tecnica di Ivanissevich. Questi approcci sono impiegati prevalentemente nei varicoceli molto voluminosi e nei pazienti in età pediatrica e adolescenziale
- legatura e sclerotizzazione delle vene spermatiche per via subinguinale: nella maggior parte dei varicocele in pazienti adulti, si propone una tecnica con incisione poco sopra la sacca scrotale, l’isolamento delle vene del funicolo e la iniezione di una sostanza sclerosante che le oblitera interrompendola in questo modo il reflusso di sangue (tecnica di Tauber o di Marmar modificata). La percentuale di complicanze e recidive, nella nostra lunga esperienza, risulta sovrapponibile alla tecnica microchirurgica.
- legatura microchirurgica con incisione inguinale (tecnica sec, Marmar): questa tecnica rappresenta il gold-standard secondo le Linee Guida internazionali (Eutropean Association of Urology – EAU, 2024) relativamente a efficacia e ridotta percentuale di complicanze. Come svantaggio tuttavia, presenta maggiori tempi operatori e la necessità di una strumentazione specifica.
TECNICA PERCUTANEA
La scleroembolizzazione radiologica percutanea non comporta un taglio chirurgico ma un accesso vascolare percutaneo, in genere attraverso la vena brachiale o succlavia destra, con esecuzione di una flebografia del sistema venoso di sinistra e, ove possibile, la interruzione del reflusso venoso mediante introduzione di sostanza sclerosante o piccole spirali.
Selezione degli spermatozoi per fecondazione in vitro
In caso di elevata frammentazione del DNA spermatico, è possibile procedere a selezione degli spermatozoi mediante tecnica di Microfluidica e di M.A.C.S. (vedi ‘METODICA DI SELEZIONE DEGLI SPERMATOZOI’).
Tali metodiche vengono applicate dai Biologi sul campione di liquido seminale ottenuto nel giorno del pick up degli ovociti: con tali tecniche è possibile selezionare, in buona parte dei casi, una popolazione di spermatozoi nella quale il tasso di frammentazione viene riportato a un livello fisiologico, e questa verrà utilizzata per fecondazione in vitro.
Laboratorio di Seminologia
Unitamente alle visite e alle consultazioni specialistiche, il Centro PMA di Clinica Polispecialistica San Carlo si caratterizza per una serie di attività strumentali diagnostiche.
Test seminali di primo livello
SPERMIOGRAMMA (Esame Seminale standard)
Lo spermiogramma viene eseguito con lo scopo di valutare la qualità del liquido seminale attraverso la verifica della concentrazione, della motilità e della forma degli spermatozoi.
Come confermato anche dall’Organizzazione Mondiale della Sanità (WHO), tale esame rappresenta lo strumento principale per la valutazione della fertilità maschile.
Ai fini dell’attendibilità dell’esame è fondamentale rispettare determinati parametri e seguire le istruzioni che verranno fornite dal personale del Centro PMA.
Il liquido seminale raccolto viene sottoposto inizialmente ad una valutazione “macroscopica” per la determinazione di alcune caratteristiche fisico-chimiche, in particolare l’aspetto, il volume, il pH, la viscosità. Successivamente viene effettuata la valutazione “microscopica” per la determinazione della concentrazione, della motilità, della morfologia e della vitalità degli spermatozoi, parametri principali che determinano la qualità dello sperma (vedi Infertilità maschile).
I risultati dello spermiogramma possono evidenziare:
Oligozoospermia: ridotta concentrazione di spermatozoi per ml
Astenozoospermia: ridotto numero di spermatozoi motili o con ridotta motilità
Teratozoospermia: ridotto numero di spermatozoi con forma normale
Azoospermia: assenza completa di spermatozoi nel citocentrifugato del liquido seminale
Ipoposia: volume dell’eiaculato inferiore alla norma
MAR (Mixed Agglutination Reaction) Test: Ricerca degli Anticorpi anti-spermatozoi
In condizioni normali, la barriera ematotesticolare protegge gli spermatozoi dal nostro sistema immunitario. Lo sperma può in certi casi presentare anticorpi con capacità di legare gli spermatozoi.
La causa di quest’alterazione non è sempre individuabile (pregressi trauma, infezioni, o ostruzioni in atto delle vie seminali, ecc). Gli anticorpi anti-spermatozoo interferiscono in diversi momenti con la funzione spermatozoaria, come la riduzione della motilità nelle vie genitali femminili e l’impedimento della penetrazione all’interno dell’ovocita. L’Organizzazione Mondiale della Sanità (WHO) raccomanda la ricerca di questi autoanticorpi nel liquido seminale. I test più utilizzati sono il MAR-Test e l’ IBT-Test.
Il risultato viene espresso come percentuale di spermatozoi motili legati da anticorpi rispetto al numero totale di spermatozoi analizzati.
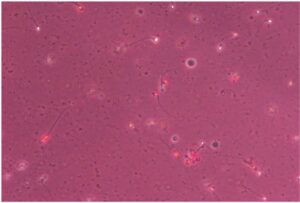
EOSIN Test
L’Eosin Test valuta la vitalità degli spermatozoi mediante una tecnica colorimetrica che si basa sul principio per cui l’eosina penetra solo all’interno degli spermatozoi non vitali, che assumeranno in questo caso la tipica colorazione rosea.
Test seminali di secondo livello
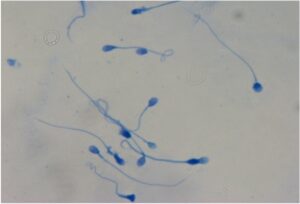
ANM (Aniline Blue) Test
Il Test al Blu di Anilina valuta il grado di maturità del nucleo degli spermatozoi.
Una elevata percentuale di spermatozoi con nucleo immaturo, che si colorano di blu, è associata ad una ridotta capacità di sviluppo dell’embrione.
Test di frammentazione del dna spermatico
Indagini biomolecolari di introduzione relativamente recente nella pratica clinica quotidiana che valutano la percentuale di spermatozoi con DNA frammentato. Questi test sono particolarmente utili al clinico nel giudizio prognostico di fertilizzazione e di abortività spontanea.
Quelli da noi eseguiti sono due: AO (Acridine Orange) ed Halosperm.
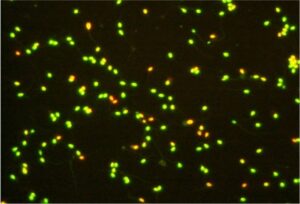
AO (Acridine Orange) Test
Il Test all’Arancio di Acridina valuta la percentuale di DNA denaturato a singola catena all’interno del nucleo dello spermatozoo. In questa procedura la testa degli spermatozoi con elevata quantità di DNA denaturato si colora di arancio, mentre gli spermatozoi normali si colorano di verde. La presenza di alterazioni del DNA in una percentuale elevata degli spermatozoi è associata a ridotta o mancata capacità di sviluppo dell’embrione.
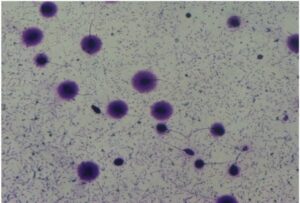
Halosperm
Il test si basa sul principio della dispersione della cromatina (SCD) degli spermatozoi.
Test diagnostico che permette di misurare i livelli di frammentazione del DNA nel liquido seminale in modo semplice, rapido e riproduciblie.
Attraverso una tecnica non invasiva che analizza spermatozoi da eiaculato, al termine del protocollo si procede con la colorazione del campione sul vetrino e l’osservazione al microscopio a luce diretta o a fluorescenza.
L’immagine visualizzata al microscopio, permette una rapida classificazione dei nuclei degli spermatozoi, in base alla presenza/dimensione o assenza dell’alone periferico di cromatina dispersa.
Tecniche di selezione degli spermatozoi
Tecniche proposte in caso di elevato indice di frammentazione del DNA spermatico:
MACS
Tecnica che consente di selezionare gli spermatozoi che non presentano danni o segni di apoptosi (morte cellulare) per poi utilizzarli nelle tecniche di riproduzione assistita.
La tecnica MACS (Magnetic Activated Cell Sorting) permette di selezionare gli spermatozoi con il DNA integro grazie a una selezione immunomagnetica separando gli spermatozoi sani da quelli morti o con DNA frammentato.
Microfluidica
La selezione degli spermatozoi con microfluidica permette di selezionare gli spermatozoi che presentano caratteristiche qualitative ottimali per il trattamento di procreazione medicalmente assistita attraverso membrane selettive, riducendo il numero di spermatozoi con DNA frammentato.
IUI (Inseminazione Intra Uterina)

L’ inseminazione intrauterina (IUI) costituisce il I livello delle tecniche di fecondazione assistita.
È la tecnica più semplice e consente di aumentare le chance di concepimento introducendo il liquido seminale precedentemente trattato direttamente in utero, superano il collo uterino e raggiungendo le tube, sede della fecondazione dell’ovocita.
Le principali indicazioni sono:
- infertilità idiopatica
- infertilità da fattore maschile di grado lieve
- endometriosi I-II stadio
- fattore cervicale
- alterazioni ovulatorie
- sindrome dell’ovaio policistico
L’inseminazione può essere eseguita su ciclo spontaneo oppure con una leggera stimolazione ormonale volta a supportare farmacologicamente la maturazione follicolare con farmaci orali o iniettabili.
La procedura consiste nel monitoraggio ecografico dell’ovulazione attraverso ecografie transvaginali e prelievi di sangue per il controllo dei valori ormonali per stabilire il momento migliore per l’inseminazione.
Il giorno dell’inseminazione si prepara il liquido seminale attraverso metodiche biologiche atte ad ottenere una piccola quantità di materiale seminale di qualità ottimale che viene depositato in utero mediante una speciale cannula flessibile.
Fecondazione in Vitro e Coltura Embrionaria
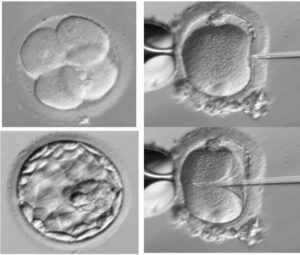
Gli ovociti prelevati al Pick up possono essere inseminati mediante tecnica FIVET o ICSI:
- Nella tecnica FIVET(Fecondazione in Vitro ed Embryo-Transfer) i gameti femminili e i gameti maschili vengono posti in una piastra contenente terreno di coltura idoneo e viene lasciata allo spermatozoo più competente la possibilità di penetrare l’ovocita in modo “naturale”;
- Nella tecnica ICSI(Intra Cytoplamatic Sperm Injection) un singolo spermatozoo viene introdotto all’interno dell’ovocita tramite un sistema di micromanipolazione.
Questa è la tecnica di elezione per i casi di infertilità maschile grave, oppure nei casi di mancata o ridotta fecondazione in seguito a tecnica FIVET.
Dopo circa 18 ore dal momento dell’inseminazione è possibile valutare l’avvenuta fecondazione degli ovociti, la coppia verrà informata del numero di ovociti fecondati dai biologi il giorno successivo al Pick Up.
Gli embrioni ottenuti verranno tenuti in coltura e trasferiti nella cavità uterina sotto guida ecografica tramite un sottile catetere.
Il trasferimento degli embrioni può essere effettuato:
- in seconda o terza giornata allo stadio di clivaggio;
- in quinta/sesta giornata allo stadio di blastocisti.
Considerati i miglioramenti nelle condizioni di coltura e nelle strumentazioni di laboratorio, allo stato attuale è possibile e consigliabile procedere alla coltura degli embrioni in vitro fino al 5°-6° giorno dal momento del Pick up, ossia fino allo stadio di blastocisti, qualora le condizioni lo consentano.
Ciò permette di garantire una migliore sincronia tra stadio embrionario ed endometrio, e permette, dato il maggior tasso di impianto delle blastocisti, di effettuare il trasferimento di un singolo embrione, evitando così il rischio di gravidanze gemellari.
Crioconservazione di Gameti ed Embrioni
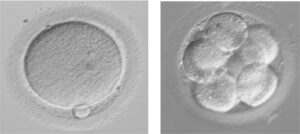
CRIOCONSERVAZIONE DEGLI OVOCITI
Le principali condizioni in cui può essere indicata la crioconservazione degli ovociti nel contesto di un ciclo di PMA sono le seguenti:
- presenza di ovociti in sovrannumero rispetto a quelli da utilizzare al fine di ottenere il numero adeguato di embrioni da trasferire idoneo a garantire il miglior risultato alla coppia (come da Sentenza della Corte Costituzionale n 151/09);
- rischio di iperstimolazione ovarica: si crioconservano tutti gli ovociti prodotti in seguito alla stimolazione, per poi procedere allo scongelamento e alla inseminazione degli stessi durante un successivo ciclo;
- indisponibilità di gameti maschili per l’inseminazione il giorno del prelievo ovocitario;
- irregolarità dell’endometrio o rialzo del progesterone (per cui si avrebbe un aumentato rischio di fallimento dell’impianto degli embrioni prodotti e trasferiti);
- considerazioni etico-religiose personali delle coppie che non desiderano ottenere e crioconservare eventuali embrioni sovrannumerari.
CRIOCONSERVAZIONE DEGLI EMBRIONI
Le principali indicazioni alla crioconservazione degli embrioni* sono le seguenti:
- problematiche cliniche a carico della paziente che non permettono di effettuare l’embryo-transfer nel medesimo ciclo di stimolazione;
- produzione di embrioni sovrannumerari rispetto al numero effettivo di embrioni da trasferire;
- necessità di posporre il transfer, come nei casi di rischio di iperstimolazione ovarica (OHSS).
La crioconservazione embrionaria consente di aumentare i tassi di gravidanza cumulativa evitando ripetute stimolazioni ovariche.
Sia per gli ovociti che per gli embrioni la metodica in uso da tempo per la crioconservazione è la vitrificazione, cioè il metodo ultrarapido di crioconservazione in cui le cellule passano da 37°C a -196°C in meno di 1 secondo.
Vista la grande efficacia e le elevate percentuali di sopravvivenza e di successo riportate in letteratura, la vitrificazione è ormai la metodica più utilizzata, ed è quella con cui vengono crioconservati ovociti ed embrioni presso il Centro PMA di Clinica Polispecialistica San Carlo.
*La Sentenza della Corte Costituzionale n. 151 del 2009, in deroga al principio generale del divieto di crioconservazione, consente la crioconservazione degli embrioni fino alla data del trasferimento, da realizzare non appena possibile.
CRIOCONSERVAZIONE DEGLI SPERMATOZOI
La crioconservazione in azoto liquido permette di conservare gli spermatozoi per un tempo indefinito e rappresenta pertanto un utile strumento di preservazione della fertilità. Alcune delle Indicazioni alla crioconservazione degli spermatozoi ono le seguenti:
- uomini affetti da severa oligozoospermia che vedono progressivamente decrescere la loro fertilità nel tempo, fino a rischiare l’azoospermia;
- uomini che devono essere sottoposti a terapie mediche (chemioterapia, radioterapia) o chirurgiche (prostatectomia) che potrebbero danneggiare la fertilità;
- uomini che per motivi professionali sono esposti a sostanze genotossiche;
- uomini affetti da azoospermia (ostruttiva o secretoria) che sono stati sottoposti con esito positivo al recupero chirurgico di spermatozoi dai testicoli (TESE, MicroTESE).
Per contattare la PMA
- centropma@clinicasancarlo.it
- Clinica Polispecialistica San Carlo - Via Ospedale, 21 - Paderno Dugnano (MI) Edificio H - Piano 1 Per prenotazioni esami seminali scrivere a: andrologia@clinicasancarlo.it
ATTENZIONE è importante lasciare i propri recapiti telefonici per essere ricontattati.
BERNASCONI ELENA
Ginecologia e Ostetricia

CASTIGLIONI FABRIZIO
Specialista in Urologia - Responsabile Area Andrologica
CASTORINA PIERANGELA
Genetica medica
COLOMBO FRANCESCA
Ginecologia e Ostetricia
DOLDI NICOLA
Ginecologia e Ostetricia
GANDOLFI ANDREA
Ginecologia e Ostetricia
GOGGI GIOVANNI
Endocrinologia e Malattie del Ricambio
SARAIS VERONICA
Ginecologia e Ostetricia
COTTI LAURA
Psicologia
TESTA PATRIZIA
Biologa
CAMINITI GIUSEPPE
Biologo
MONTI VALENTINA
Biologa, Referente Qualità Centro PMA
SANTOLI MARCO
Biologo
AMBROGGI BEATRICE
Ostetrica
BORRONI PAOLA
Ostetrica
MIRANDA SILVIA
Ostetrica
MASCIOCCHI FEDERICA
Ostetrica